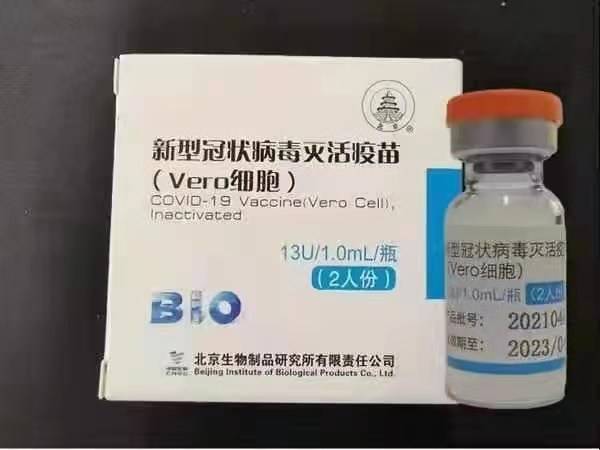
Sinopharm (Pechino): BBIBP-CorV
FASE 1
1 prova
ChiCTR2000032459
Cina
FASE 2
2 prove
NCT04962906
Argentina
ChiCTR2000032459
Cina
FASE 3
6 prove
NCT04984408
ChiCTR2000034780
Emirati Arabi Uniti
NCT04612972
Perù
NCT04510207
Bahrain, Egitto, Giordania, Emirati Arabi Uniti
NCT04560881, BIBP2020003AR
Argentina
NCT04917523
Emirati Arabi Uniti
Approvazioni
Elenco degli usi di emergenza dell'OMS 59 Paesi
Angola、Argentina、Bahrain、Bangladesh、Bielorussia、Belize、Bolivia (Stato Plurinazionale di)、Brasile、Brunei Darussalam、Cambogia、Camerun、Ciad、Cina、Comore、Egitto、Guinea Equatoriale、Gabon、Gambia、Georgia、Guyana、Ungheria、ndonesia Iran (Repubblica Islamica di)、Iraq、Giordania、Kirghizistan、Repubblica Democratica Popolare del Laos
Libano、Malesia、Maldive、Mauritania、auritius、Mongolia、Montenegro、Marocco、Mozambico、Namibia、Nepal、Niger、Macedonia del Nord、Pakistan、Paraguay、Perù、Filippine、Repubblica del Congo、enegal、Serbia、Seychelles、Sierra Leone、Solo Isole、Somalia、Sri Lanka、Thailandia、Trinidad e Tobago、Tunisia、Emirati Arabi Uniti、Venezuela (Repubblica Bolivariana di)、Viet Nam、Zimbabwe
Sinopharm BBIBP-CorV COVID-19 è un vaccino inattivato a base di particelle virali coltivate in coltura prive di capacità patogena. Questo candidato vaccino è stato sviluppato da Sinopharm Holdings e dall'Istituto di prodotti biologici di Pechino.
Il vaccino Sinopharm BBIBP-CorV funziona consentendo al sistema immunitario di produrre anticorpi contro il beta coronavirus SARS-CoV-2. I vaccini a virus inattivati sono stati utilizzati per decenni, come il vaccino contro la rabbia e il vaccino contro l'epatite A. Questa tecnologia di sviluppo è stata applicata con successo a molti vaccini noti, come il vaccino contro la rabbia.
Il ceppo SARS-CoV-2 di Sinopharm (ceppo WIV04 e numero di libreria MN996528) è stato isolato da un paziente dell'ospedale Jinyintan di Wuhan, in Cina. Il virus è stato propagato in coltura in una linea cellulare competente Vero e il surnatante delle cellule infette è stato inattivato con -propiolattone (1:4000 vol/vol, da 2 a 8°C) per 48 ore. Dopo la chiarificazione dei detriti cellulari e l'ultrafiltrazione, è stata eseguita una seconda inattivazione del β-propiolattone nelle stesse condizioni della prima inattivazione. Secondo l'OMS, il vaccino è stato adsorbito su 0,5 mg di allume e caricato in siringhe preriempite in 0,5 ml di soluzione salina sterile tamponata con fosfato senza conservanti.
Il 31 dicembre 2020, la State Drug Administration ha annunciato l'approvazione del vaccino sperimentale sviluppato da Sinopharm.
Il 7 maggio 2021, l'Organizzazione mondiale della sanità ha annunciato l'approvazione del vaccino. L'elenco degli usi di emergenza dell'OMS ha consentito ai paesi di accelerare le proprie approvazioni normative per importare e somministrare il vaccino COVID-19. Anche il gruppo consultivo di esperti dell'OMS sulle strategie di immunizzazione ha completato la revisione del vaccino. Sulla base di tutte le prove disponibili, l'OMS raccomanda due dosi di vaccino, a distanza di tre o quattro settimane, per gli adulti dai 18 anni in su. L'efficacia del vaccino contro la malattia sintomatica e ospedaliera è stimata al 79% per tutti i gruppi di età messi insieme.
L'American Medical Association ha pubblicato "A Randomized Clinical Trial: Effect of 2 Inactivated SARS-CoV-2 Vaccines on Symptomatic COVID-19 Infection in Adults" il 26 maggio 2021, concludendo che "in questa analisi ad interim prespecificata di uno studio clinico randomizzato, adulti I 2 vaccini SARS-CoV-2 inattivati somministrati in questa analisi ad interim prespecificata di studi clinici randomizzati hanno ridotto significativamente il rischio di COVID-19 sintomatico e gli eventi avversi gravi sono stati rari". In questo studio randomizzato di fase 3 negli adulti, l'efficacia dei 2 vaccini virali interi inattivati nei casi sintomatici di COVID-19 è stata rispettivamente del 72,8% e del 78,1%. 2 vaccini hanno avuto eventi avversi gravi rari con frequenza simile al gruppo di controllo con solo allume e la maggior parte non era correlata alla vaccinazione. Un'analisi esplorativa ha rilevato che i 2 vaccini hanno indotto anticorpi neutralizzanti misurabili, simili ai risultati dello studio di fase 1/2.
Il 10 maggio 2021 il gruppo di lavoro SAGE dell'OMS ha pubblicato una revisione del vaccino Sinopharm/BBIBP COVID-19. Il vaccino COVID-19 di GAVI incorpora un monitor di fiale di vaccino che informa gli operatori sanitari se il vaccino è stato conservato correttamente e non è stato esposto a surriscaldamento. Di conseguenza, GAVI ha riferito il 14 maggio 2021. Le etichette intelligenti prodotte da Zebra Technologies e realizzate da Temptime Corporation, sono costituite da un cerchio con un quadrato di colore più chiaro al centro, costituito da una sostanza chimica incolore che sviluppa colore irreversibilmente nel tempo . Questo diventa più scuro per dare un'indicazione visiva dell'esposizione cumulativa al calore. Una volta che la fiala è stata esposta al calore oltre il suo intervallo di conservazione ottimale, il quadrato diventa più scuro del cerchio, indicando che il vaccino non deve più essere utilizzato.
National Drug BBIBP-CorV Numero di registrazione della libreria dei farmaci per i vaccini COVID-19: DB15807.